L'atome – Nucléides et radio-isotopes
L'atome, le fondement de la matière
Toute la matière qui nous entoure est composée d'atomes. Les atomes forment des éléments comme l'oxygène, l'hydrogène et le carbone.
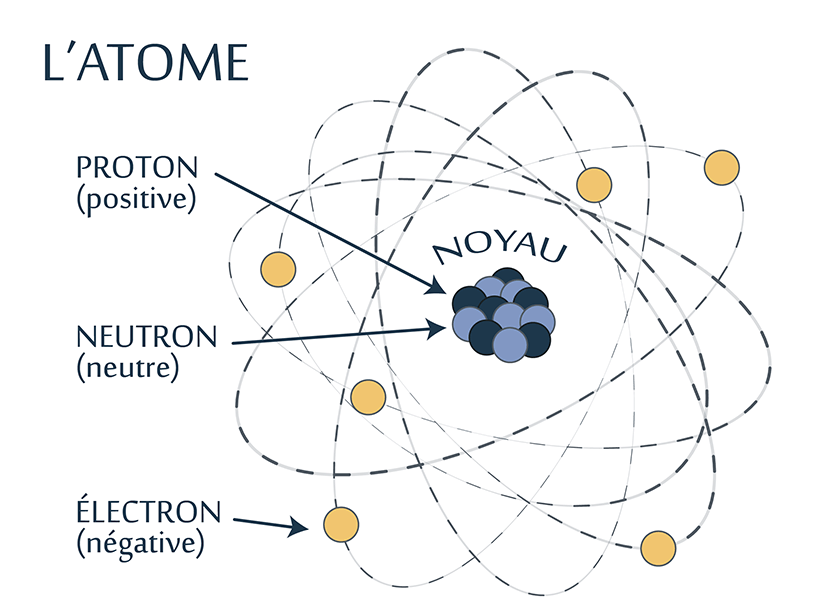
Un atome
Un atome est composé de protons et de neutrons, qui forment le noyau, et d’électrons, qui gravitent autour du noyau. Le noyau porte une charge positive; les protons sont chargés positivement, alors que les neutrons sont neutres électriquement, comme leur nom l’indique. Les électrons sont des particules chargées négativement qui se déplacent autour du noyau en formant un nuage périphérique. Les électrons négatifs sont attirés vers le noyau positif par une force électrique. C’est grâce à cette attraction que les électrons restent en orbite autour du noyau.

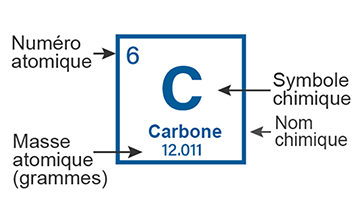
Le nombre de protons dans le noyau, ou numéro atomique, permet de différencier les éléments chimiques entre eux. Chaque élément possède un nombre unique de protons. Par exemple, il y a six protons dans le carbone; pour cette raison, son numéro atomique est 6 dans le tableau périodique des éléments.
Les atomes sont stables lorsque le nombre de neutrons dans le noyau est à peu près équivalent au nombre de protons. Lorsqu'il y a un déséquilibre important entre le nombre de neutrons et celui de protons dans le noyau, l'atome devient instable. Pour retrouver sa stabilité, il peut subir une transformation ou désintégration radioactive.
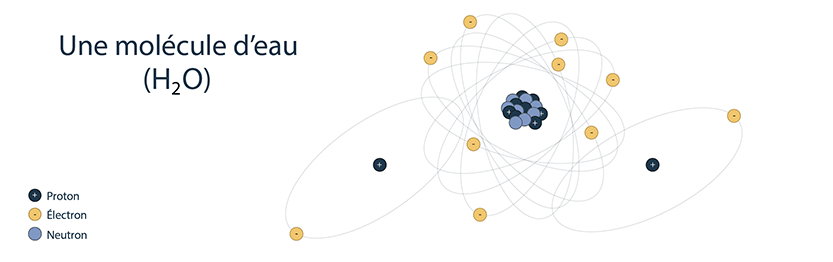
Les atomes d'un ou de plusieurs éléments se combinent entre eux pour former des composés plus volumineux portant le nom de molécules. Une molécule d'eau, par exemple, est constituée de deux atomes d'hydrogène combinés à un atome d'oxygène (H2O).
Le nucléide
Un nucléide est une entité atomique caractérisée par le nombre de protons et de neutrons qui composent le noyau, lequel correspond approximativement à la masse du nucléide. Le numéro qui accompagne parfois le nom du nucléide est le nombre de masse (somme des protons et des neutrons dans le noyau). Par exemple, le carbone 12 est un nucléide de carbone avec 6 protons et 6 neutrons.
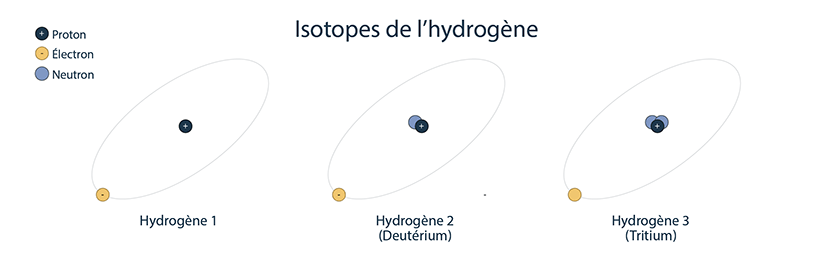
Comprendre les isotopes
Les nucléides d’un élément qui ont le même nombre de protons mais un nombre différent de neutrons sont appelés des isotopes de cet élément. Il s’agit de variantes du même élément de base. Par exemple, il existe trois isotopes (ou variantes) de l’hydrogène : l’hydrogène 1 (un proton et aucun neutron), l’hydrogène 2 ou deutérium (un proton et un neutron) et l’hydrogène 3 ou tritium (un proton et deux neutrons). D’autres exemples : l’uranium 235, qui possède 92 protons et 143 neutrons, ainsi que l’uranium 238, qui possède 92 protons et 146 neutrons. L’uranium 235 et l’uranium 238 sont tous deux des isotopes de l’uranium.
L’isotope stable
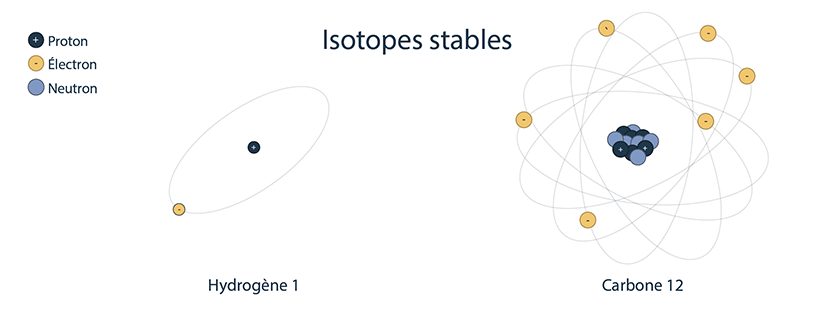
De nombreux isotopes sont stables. Ils ne subissent pas de désintégration radioactive et n’émettent pas de rayonnement. D’autres isotopes sont instables. Un isotope est stable lorsqu’il y a un équilibre entre le nombre de neutrons et le nombre de protons. Lorsqu’un isotope est petit et stable, il contient pratiquement le même nombre de protons que de neutrons. Les isotopes stables plus volumineux ont légèrement plus de neutrons que de protons.
Parmi les isotopes stables figure le carbone 12, soit six protons et six neutrons, pour une masse totale de 12 grammes.
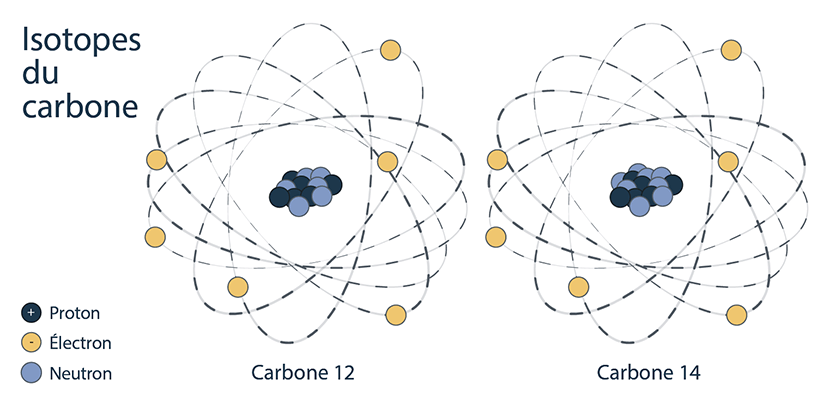
L’isotope instable
Lorsqu’il y a un déséquilibre entre le nombre de protons et de neutrons, habituellement lorsque le ratio entre neutrons et protons est trop bas, l’isotope voudra se transformer en forme plus stable, c’est à dire en atome différent. Lorsque ce phénomène se produit, l’atome réduit sa masse en émettant des particules alpha, des particules bêta, des positrons et/ou des rayons gamma, mais certains pourront atteindre la stabilité par fission spontanée ou capture d’électrons. Il s’agit d’un processus spontané qui porte le nom de désintégration radioactive.
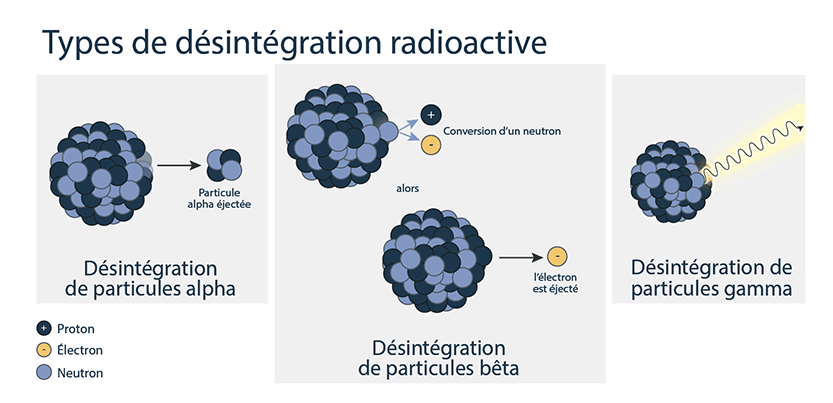
Il existe trois grands types de désintégration radioactive :
Désintégration alpha : Lorsqu’un atome subit une désintégration alpha, il éjecte du noyau une particule composée de deux protons et de deux neutrons, ce qui a pour résultat que le numéro atomique diminue de deux et la masse diminue de quatre.
Désintégration bêta : La désintégration bêta se produit lorsqu’un neutron dans le noyau d’un atome instable se convertit en proton et qu’un électron est éjecté du noyau. Le numéro atomique augmente de un, mais la masse ne diminue que légèrement.
Désintégration gamma : La désintégration gamma est la libération de l’énergie excédentaire présente dans le noyau après une désintégration alpha ou bêta, ou après la capture des neutrons dans un réacteur nucléaire. L’énergie résiduelle est émise sous forme de photon de rayons gamma. La désintégration gamma n’affecte généralement pas la masse ni le numéro atomique du radio-isotope.
Radioactivité
Lorsqu’un isotope se désintègre spontanément, l’énergie excédentaire qui est émise est une forme de rayonnement ionisant. Autrement dit, la désintégration émet un rayonnement, ce qui porte le nom d’activité. L’isotope qui se transforme et émet un rayonnement porte le nom de radio-isotope.
La désintégration est exprimée ou mesurée en unités appelées becquerels (Bq). Un becquerel correspond à une désintégration par seconde.
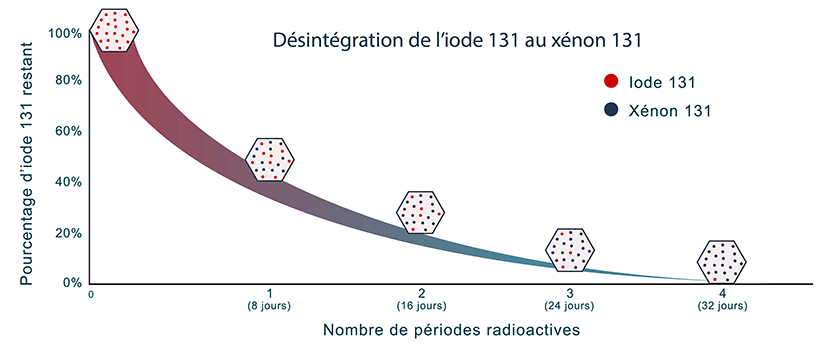
Période radioactive
La période radioactive est le temps nécessaire pour que l’activité d’un radio-isotope soit réduite de moitié par un processus de décroissance radioactive. Son symbole est t½. Chaque radio-isotope a une période unique qui peut varier entre une fraction de seconde et plusieurs milliards d’années.
Par exemple, la période radioactive de l’iode 131 est de huit jours, alors qu’elle est de 24 000 ans pour le plutonium 239.
Si la source originelle de la radioactivité est connue, il est possible de calculer le temps nécessaire à sa désintégration. L’inverse est également vrai. Si la période radioactive est connue, il est alors possible d’identifier le radio-isotope.
Activité massique
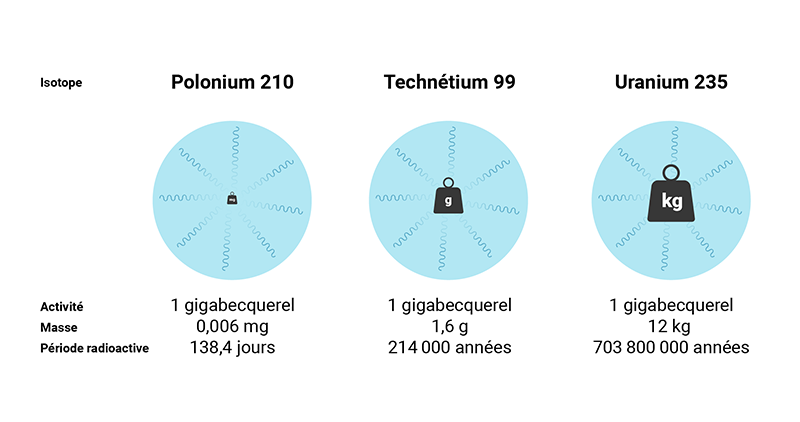
L’activité massique désigne l’activité (la vitesse de désintégration d’un isotope radioactif) par unité de masse d’un radio-isotope. Il existe une relation inversement proportionnelle entre la période radioactive et l’activité massique :
- Les isotopes qui possèdent une plus longue période radioactive, comme l’uranium 238, se désintégreront plus lentement et émettront moins de rayonnement par seconde par gramme.
- Les isotopes qui ont une période radioactive plus courte, comme le cobalt 60, se désintégreront plus rapidement et émettront plus de rayonnement par seconde par gramme.
Prenons par exemple un gramme de cobalt 60 et un gramme d’uranium 238 : à quantité égale, le cobalt 60 émettra beaucoup plus de rayonnement pendant une période beaucoup plus courte que l’uranium 238.
Le tableau suivant présente une comparaison entre différents radio-isotopes ayant différentes périodes radioactives et montre la relation inverse entre la période radioactive et l’activité massique. La dernière colonne, « Milligrammes par MBq », indique la quantité d’isotopes requise en milligrammes pour obtenir un mégabecquerel d’activité. L’activité massique est exprimée en becquerels par gramme, et l’activité massique de chaque radio-isotope dépend de sa période radioactive ainsi que de sa masse atomique.
| Radio-isotope | Période radioactive | Activité massique (Bq/g) | Milligrammes (mg) par MBq |
|---|---|---|---|
| Polonium 210 | 138,4 jours | 166,3E 12 (166,3 TBq/gr) | 0,000 006 |
| Cobalt 60 | 5,3 années | 41,9E 12 (41,9 TBq/gr) | 0,000 0239 |
| Césium 137 | 30,04 années | 3,2E 12 (3,2 TBq/gr) | 0,000 3109 |
| Carbone 14 | 5 700 années | 165,7E 9 (165,7 GBq/gr) | 0,006 |
| Technétium 99 | 214 000 années | 624,9E 6 (624,9 MBq/gr) | 1,6 |
| Uranium 235 | 703 800 000 années | 80,0E 3 (80,0 kBq/gr) | 12 000,5 |
| Uranium 238 | 4 468 000 000 années | 12,4E 3(12,4 kBq/gr) | 80 000,4 |
Sources naturelles et artificielles de radio-isotopes
Il existe de nombreuses sources naturelles de radio-isotopes. Leur origine remonte à la formation du système solaire et résulte des interactions entre les rayons cosmiques et les molécules dans l’atmosphère. Le tritium, par exemple, résulte de l’interaction entre les rayons cosmiques et des molécules atmosphériques. Certains des radio-isotopes qui se sont formés au même moment que notre système solaire ont des périodes de plusieurs milliards d’années et continuent d’être présents dans notre environnement. L’uranium et le thorium en sont des exemples.
L’humain produit également des radio-isotopes dans les réacteurs nucléaires et dans les générateurs de radio-isotopes comme les cyclotrons. Plusieurs radio-isotopes de sources artificielles sont utilisés en médecine nucléaire, en biochimie, par l’industrie de la fabrication et en agriculture.
Renseignements complémentaires
Détails de la page
- Date de modification :